溴化亞錫
物理性質
性狀:黃色晶體。
密度(g/mL,20℃):5.12
熔點(oC):232
沸點(oC,常壓):620
溶解性:溶于水。
作用與用途
可溶于水、乙醇、乙醚、丙酮,其稀水溶液會發生水解。
合成方法
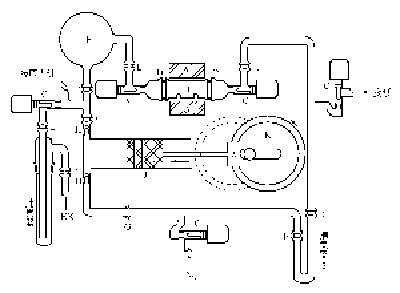
圖XIV-23 制備溴化亞錫的循環系統
1.燒瓶中加入粉末狀錫和濃氫溴酸,在砂浴上加熱至氫氣發生結束,過濾分離除去未反應的錫。將濾液與少量的錫箔共同在水浴上加熱濃縮至少量的鹽析出。冷卻后析出黃色針狀結晶,迅速用玻璃砂芯漏斗進行抽濾,結晶放在素瓷板上置于盛有濃硫酸的真空干燥器中干燥。待結晶還濕潤時,將其移至燒瓶中,在氮氣氛下直接用火加熱,加熱逐漸由弱至強,最初產生水,接著溴化氫加合物分解產生溴化氫。當停止產生氣體時,形成SnBr2的透明熔融體,在氮氣流中冷卻。產物可用石英蒸餾瓶在氮氣流中蒸餾精制。
2.反應原理同制法1。設計一個循環裝置,讓適量的HBr氣體通過熔化的錫上方生成SnBr2。SnBr2受熱升華,凝結在較冷的反應管兩端。而不斷暴露出的錫表面繼續與HBr反應,這是一個半自動化的合成方法。
圖中裝置均用硼硅酸耐熱玻璃制作,所有的接口和活塞都帶O形密封圈,材質為聚四氟乙烯。活塞大小與直徑25mm氣缸相配。用帶有藍寶石珠的毛玻璃止逆閥作氣閥。活塞涂黃油潤滑。驅動活塞的電機用110V交流電,3600r/min,換低速擋600∶1。活塞通過偏心輪連接推桿,沖程為2.54cm。
圖制備溴化亞錫的循環系統
A—管式爐;B—反應管;C—聚四氟乙烯塞;D—15mm O形接口;
E—9mm O形接口;F—平衡容器;G—9mm球窩連接器;
H—止逆閥;I—玻璃氣缸;J—聚四氟乙烯噴槍;K—偏心輪
將市售的錫粒在石英燒瓶中加熱熔化后傾倒入一支大玻璃試管中,除去表面粗糙的氧化產物。冷卻后取出錫,并將錫切割成如同反應器大小。反應器(B)是可拆卸的,將錫放入其中的玻璃凹槽間,大致10g,將系統連接好,開泵抽真空,在280℃下保持1h。捕集器1保持在-78℃,讓HBr氣體充滿系統達101325kPa。為了除去不可冷凝的氣體,HBr氣在-196℃的捕集器2中冷凝,系統再被抽真空。然后體系關閉,將捕集器2升溫至25℃,活塞開始工作,HBr氣體逐漸被H2取代,約12h后被耗盡,停活塞,捕集器2再冷卻到-196℃,剩余反應物又冷凝在此,可卸下捕集器2,H2用泵抽走。關掉往復泵,體系在真空下運轉,反應器在280℃保溫1h,產品升華,直至錫表面不再有SnBr2產品,然后冷卻系統,關閉聚四氟乙烯塞,隔離反應部分,卸下反應管,將產品回收到干燥器中。
HBr的用量由系統的體積和壓力估算出,反應中錫是過量的。一次實驗中得到4.0gSnBr2,產率達70%。
毒理學數據
可能引起的刺激影響:
在皮膚上面:可能引起發炎
在眼睛上面:可能引起發炎
生態學數據
通常對水體是稍微有害的,不要將未稀釋或大量產品接觸地下水,水道或污水系統,未經政府許可勿將材料排入周圍環境。
計算化學數據
計算化學數據:
1、 疏水參數計算參考值(XlogP):未確定
2、 氫鍵供體數量:0
3、 氫鍵受體數量:2
4、 可旋轉化學鍵數量:0
5、 拓撲分子極性表面積(TPSA):0
6、 重原子數量:3
7、 表面電荷:0
8、 復雜度:0
9、 同位素原子數量:0
10、 確定原子立構中心數量:0
11、 不確定原子立構中心數量:0
12、 確定化學鍵立構中心數量:0
13、 不確定化學鍵立構中心數量:0
14、 共價鍵單元數量:3








