硅烷
物理性質
性狀:無色氣體,有大蒜惡心氣味。
密度(g/mL,25°C):1.44
相對蒸汽密度(g/mL,空氣=1):1.1
熔點(oC):-185
沸點(oC,常壓):-111.9
沸點(oC,760mmHg):-112
蒸發熱(KJ/mol):12.5
熔化熱(KJ/mol):0.67
生成熱(KJ/mol):32.6
比熱容(KJ/(kg·K),25oC):1.335
臨界溫度(oC):-3.5
臨界壓力(MPa):4.864
溶解性:溶于水,幾乎不溶于乙醇、乙醚、苯、氯仿、硅氯仿和四氯化硅。
作用與用途
避免強氧化劑,強堿,鹵素。標準狀態下氣體密度為1.44g/L,液體的相對密度為0.68(-185℃)。蒸氣壓11mmHg(1mmHg=133.322Pa)(-160℃)、102mmHg(-140℃)、470mmHg(-120℃)。紅外光譜波長2191cm-1、914cm-1。在室溫時為氣體狀態,在儲存過程中,數月之內無顯著分解。因為甲硅烷幾乎不溶于潤滑脂,可以儲存在瓶塞涂有潤滑脂的容器內。
化學性質:硅烷的化學性質比烷烴活潑得多,極易被氧化。在與空氣接觸時可發生自燃。25℃以下與氮不起作用,室溫下與烴類化合物不起反應。與氧反應異常激烈,即使在-180℃溫度下也會猛烈反應。
硅烷與氟氯烴類滅火劑會發生激烈反應,所以不能用這類滅火劑滅火。爆炸極限為0.8%~98%。
性質與穩定性
1.電子工業用作氮化硅、外延材料等的摻雜源。半導體超純硅原料,是半導體工業中單晶硅、多晶硅外延片以及二氧化硅、氮化硅、磷硅玻璃等化學氣相沉積工藝的硅源,并廣泛用于太陽能電池、硅復印機鼓、光電傳感器、光導纖維及特種玻璃等的生產研制。
2. 用于電子工業中多晶硅和單晶硅外延淀積、二氧化硅的低溫化學氣相沉積、非晶硅薄膜淀積。
合成方法
1.如圖組裝裝置。在反應瓶和加料漏斗里分別裝入1.14g LiAlH4于70mL乙醚中的溶液和2.30mL SiCl4于50mL乙醚中的圖硅烷的制備裝置溶液。在整個合成過程中,把冷浴和指型冷卻管分別保持在-15~-20℃和-78.5℃。將儀器抽空后,乙醚開始回流,此時必須要注意避免過多的驟沸。然后,將靠近反應裝置的U形管接收器冷卻到-95℃(用甲苯凍膏),其余四個接收器冷卻到-196℃(液氮)。在攪拌下,用15min將SiCl4+乙醚溶液加入到LiAlH4懸浮液中。為了避免乙醚劇烈回流,使甲硅烷連續地以中等速度分出。調節反應器和真空管路之間的玻璃活塞便可以容易地控制反應速度。將SiCl4加完后,繼續攪拌15~20min,以保證反應完全。在此期間,將反應器和真空系統切斷以免乙醚逃逸過多。當甲硅烷從真空系統排凈之后,將空氣通入反應器,拆開真空系統。
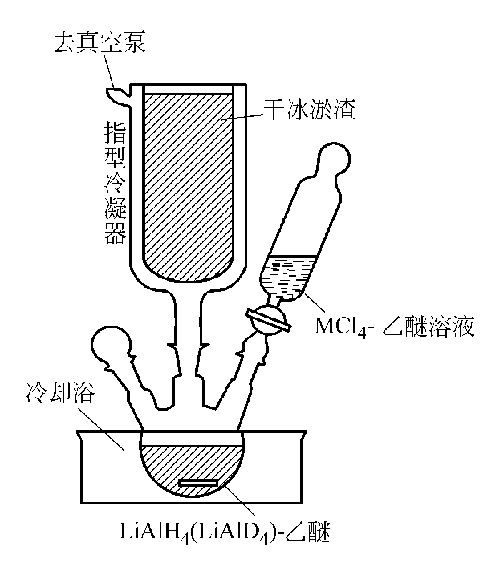
圖XIV-7 硅烷的制備裝置
從液氮冷卻的接收器中取出分離物(甲硅烷及痕量乙醚),集中到一起,將-95℃接收器接收的物料放掉(主要為乙醚)。為了除去痕量的乙醚,最好在-130℃的接收器通過5次(用戊烷冷卻),而收集在-196℃接收器中,純甲硅烷的收率為SiCl4的80%。雜質有氯化氫,此氯化氫,以-160℃接收器來代替-130℃接收器,幾乎可以完全除去。最后殘余的痕量氯化氫,用水或濕的1,2-二甲氧基乙烷處理之后,通過-130℃接收器可以除去。
圖Lely電爐
A—石墨圓筒;B—絕熱區;
C—石墨棒;D—石墨發熱體;
E—單晶成長坩堝;F—測溫
用觀察縫;G—測溫窗
貯存方法
1.貯存于干燥、陰涼、通風的庫房內。鋼瓶應該直立固定貯存。
2.要保護鋼瓶,防止極端溫度和天氣的影響。不可與易燃品、氧化劑共存混運,遠離火源。
毒理學數據
接觸硅烷眼睛會受到刺激,吸入會導致頭痛、惡心、黏膜和呼吸道的刺激。在職業環境里暴露于硅烷的閾值極限的8小時時間權重平均值(TLVTWA)為5×10-6,這已經被美國政府工業衛生學者會議(ACGIH)所確定,并被美國職業安全和健康管理局(OSHA)所采用。使用時應作好防護。
計算化學數據
1、 疏水參數計算參考值(XlogP):
2、 氫鍵供體數量:6
3、 氫鍵受體數量:6
4、 可旋轉化學鍵數量:0
5、 互變異構體數量:
6、 拓撲分子極性表面積(TPSA):121
7、 重原子數量:7
8、 表面電荷:0
9、 復雜度:62.7
10、 同位素原子數量:0
11、 確定原子立構中心數量:0
12、 不確定原子立構中心數量:0
13、 確定化學鍵立構中心數量:0
14、 不確定化學鍵立構中心數量:0
15、 共價鍵單元數量:1
安全信息
危險運輸編碼: UN 2203 2.1
危險品標志: 易燃有害
安全標識:S9 S16 S33 S36/S37/S39
危險標識:R12 R17 R20








