過氧化鈉
物理性質(zhì)
1. 沸點(diǎn)(oC,常壓):657
閃點(diǎn)(oC):657
溶解性:溶于水,溶于稀酸不溶于堿。
作用與用途
1.如果遵照規(guī)格使用和儲存則不會分解,未有已知危險反應(yīng),避免還原劑、水分/潮濕、易氧化材料、金屬粉末、酸、酸酐、硫磺、硫化物、酒精
2.在空氣中吸收水分和二氧化碳。與水發(fā)生劇烈反應(yīng)。對呼吸系統(tǒng)和皮膚有刺激性。
加熱至460℃分解。溶于稀酸,不溶于堿,在醇和氨中分解放出氧。有吸濕性,在空氣中吸收水分和二氧化碳生成氫氧化物和碳酸鹽。它本身雖不會燃燒或爆炸,但與易氧化的有機(jī)物或無機(jī)物混合能發(fā)火燃燒或爆炸。與水猛烈作用產(chǎn)生大量的熱而引起火災(zāi)。有強(qiáng)烈的腐蝕性,是一種強(qiáng)氧化劑。工作人員操作時應(yīng)穿戴勞保防護(hù)用具。灼燒至紅熱分解并放出氧氣。遇水分解生成過氧化氫H2O2。
性質(zhì)與穩(wěn)定性
1.用作分析試劑,如用作分解樣品的堿性氧化性溶劑。
2.用做氧化劑、防腐劑、除臭劑、殺菌劑、漂白劑等。也可用于制備過氧化氫。
3.用作強(qiáng)氧化劑、漂白劑、去臭劑、消毒劑和防腐劑。化學(xué)工業(yè)中用于制備其他過氧化物等。
合成方法
1.金屬鈉氧化法 將熔融金屬鈉預(yù)熱至180℃以上,向氧化爐中噴入壓力為39.2~44.1Pa的高速壓縮空氣流,在300~350℃使鈉氧化燃燒,生成的過氧化鈉經(jīng)自由沉降逐漸冷卻至100℃以下,得到過氧化鈉成品。其反應(yīng)式:
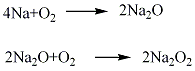
2.可用金屬鈉氧化法。 Na2O2的制備分為兩步。首先用金屬鈉在一個含氧量低于空氣的氛圍中氧化成氧化鈉,然后再將氧化鈉在含氧量比空氣高的氛圍中,加熱200~350℃進(jìn)一步氧化成 Na2O2。欲氧化徹底,第二次氧化前,先將Na2O充分粉碎。但必須隔絕濕氣。
3.將0℃的試劑氫氧化鈉飽和溶液與42%的過氧化氫按理論配比混合,進(jìn)行反應(yīng):
當(dāng)沉淀不再析出后,抽濾,然后用無水乙醇和乙醚洗滌,得特別明亮的八水合過氧化鈉。也可將工業(yè)品過氧化鈉溶于4倍冰水中,控制溫度不超過40℃,在溶液冷到0℃時析出八水合過氧化鈉結(jié)晶,過濾后抽濾,并在不含二氧化碳的空氣中干燥而制得八水合過氧化鈉。
貯存方法
1.應(yīng)貯存于陰涼、通風(fēng)、干燥的庫房中。最好是專庫專貯。
2.容器必須密封,避免日光直射,特別注意防潮、防水。
3.裝卸時要輕拿輕放,防止包裝破損。
毒理學(xué)數(shù)據(jù)
對皮膚和黏膜有強(qiáng)侵蝕性,濺入眼睛中會引起視力下降,甚至失明。
生態(tài)學(xué)數(shù)據(jù)
對是水稍微有危害的不要讓未稀釋或大量的產(chǎn)品接觸地下水、水道或者污水系統(tǒng),若無政府許可,勿將材料排入周圍環(huán)境。
計算化學(xué)數(shù)據(jù)
1、 氫鍵供體數(shù)量:0
2、 氫鍵受體數(shù)量:2
3、 可旋轉(zhuǎn)化學(xué)鍵數(shù)量:0
4、 拓?fù)浞肿訕O性表面積(TPSA):46.1
5、 重原子數(shù)量:4
6、 表面電荷:0
7、 復(fù)雜度:4
8、 同位素原子數(shù)量:0
9、 確定原子立構(gòu)中心數(shù)量:0
10、 不確定原子立構(gòu)中心數(shù)量:0
11、 確定化學(xué)鍵立構(gòu)中心數(shù)量:0
12、 不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
13、 共價鍵單元數(shù)量:3
安全信息
危險運(yùn)輸編碼: UN 1504 5.1/PG 1
危險品標(biāo)志: 氧化劑腐蝕
安全標(biāo)識:S8 S27 S39 S45
危險標(biāo)識:R8 R35
分子結(jié)構(gòu)數(shù)據(jù)
1、 摩爾折射率:121.90
2、 摩爾體積(m3/mol):465.7
3、 等張比容(90.2K):1082.9
4、 表面張力(dyne/cm):29.2
5、 極化率(10








